Ver traducción automática
Esta es una traducción automática. Para ver el texto original en inglés haga clic aquí
#Novedades de la industria
Aplicación del sistema de pletismografía de cuerpo entero (WBP)
en el estudio de la fibrosis pulmonar
Sistema de pletismografía corporal-WBP
El sistema de pletismografía de cuerpo entero puede medir los parámetros respiratorios de animales conscientes y en movimiento libre, como la frecuencia respiratoria, el volumen corriente, la hiperreactividad de las vías respiratorias (AHR), etc. Durante la prueba, el animal puede estar consciente y sin sujeción, lo que evita el impacto de la traqueotomía traumática y la anestesia, simplificando el proceso experimental. Se utiliza para estudiar la capacidad de respuesta de los animales modelo respiratorios a los fármacos y la farmacología y toxicología de los fármacos respiratorios. Es especialmente adecuado para pruebas rápidas de detección inicial de animales a gran escala, estudios de seguimiento a largo plazo y pruebas de detección repetidas. Los sistemas de pletismografía de cuerpo entero también se utilizan en el estudio de la fibrosis pulmonar.
Antecedentes
En la actualidad, la incidencia y la mortalidad de la fibrosis pulmonar aumentan año tras año. Al mismo tiempo, siguen faltando métodos de tratamiento eficaces en la práctica clínica. Diversos estudios han demostrado que las células madre mesenquimales pueden tratar la inflamación pulmonar y aliviar la progresión de la fibrosis pulmonar a través de múltiples mecanismos, como los efectos paracrinos, la transferencia mitocondrial y la inducción de la polarización de los macrófagos. Sin embargo, la terapia con células madre sigue enfrentándose a problemas como la dificultad de monitorizar las células madre tras el trasplante, el corto tiempo de retención pulmonar y la baja tasa de supervivencia.
Una nueva sonda multifuncional para la terapia con células madre
En respuesta a estos problemas, el equipo formado por el investigador Chen Hangrong y el investigador asociado Ma Ming, del Instituto de Cerámica de Shanghai de la Academia China de las Ciencias, utilizó la estrategia de "autoensamblaje multiescala inducido por metaloporfirina" para construir una nueva sonda multifuncional de ayuda a la terapia con células madre. La sonda compuesta consta de tres componentes funcionales con potencial de aplicación clínica: protoporfirina de cloruro de cobalto (CoPP), nanopartículas de oro y nanopartículas superparamagnéticas de Fe3O4. Utiliza una química de clic sin cobre para lograr un etiquetado bioortogonal eficiente de las células madre. Esta nanosonda autoensamblada no requiere portadores ni tensioactivos adicionales y puede ejercer eficazmente las funciones correspondientes de cada componente a una dosis menor. En concreto, las dos funciones de la nanosonda, la obtención de imágenes de contraste por tomografía computarizada y la manipulación magnética, resuelven respectivamente los problemas de la difícil monitorización y el corto tiempo de retención de las células madre en los pulmones; la sonda mejora eficazmente la tasa de supervivencia y el efecto reparador de las células madre mediante la liberación lenta del fármaco antioxidante CoPP en el microentorno de las células madre. Mediante la construcción de un pequeño modelo animal de fibrosis pulmonar, se confirmó que, en comparación con el grupo de tratamiento con una sola célula madre, esta terapia multifuncional con células madre mediada por nanosondas autoensambladas puede aliviar significativamente los síntomas de la fibrosis y promover la recuperación de la función pulmonar, y tiene un buen potencial de aplicación clínica.
Diagrama esquemático de la preparación de la sonda multifuncional; (b) Diagrama esquemático de la sonda utilizada para etiquetar células madre y tratar la fibrosis pulmonar; (c) Imagen TEM de la sonda multifuncional en forma de cuenco; (d) Imagen de campo oscuro anular de alto ángulo e imagen de distribución de elementos; (e) Imagen microscópica de células madre etiquetadas por la sonda multifuncional, la flecha roja indica las partículas de la sonda dentro de la célula.
Modelo de fibrosis pulmonar inducida por bleomicina
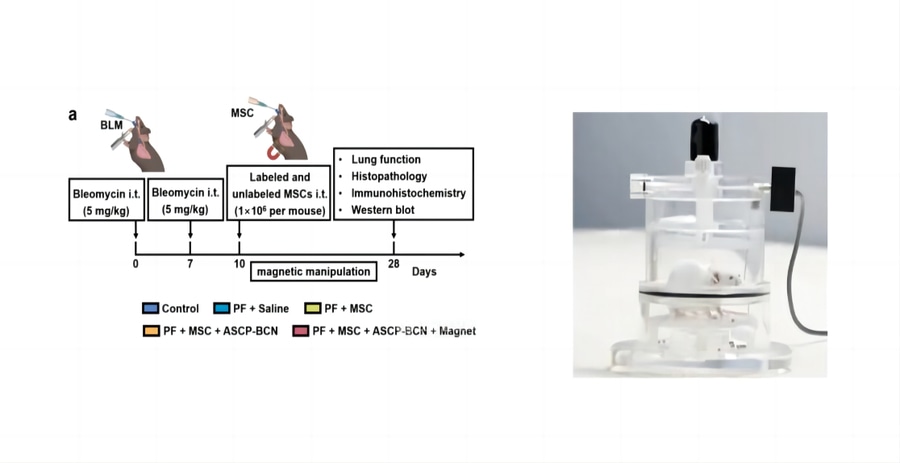
se aclimataron 36 ratones macho C57BL/6 durante 1 semana y se dividieron aleatoriamente en 6 grupos: (1) control, (2) FP, (3) FP + solución salina, (4) FP + MSC, (5) FP + MSC marcadas con ASCP-BCN, (6) FP + MSC marcadas con ASCP-BCN + imán (n = 6). La fibrosis pulmonar se indujo con bleomicina (BLM). Brevemente, se anestesió a los ratones y se disolvió BLM (5 mg/kg) en 100 μL de solución salina estéril y se inyectó lentamente en el lumen traqueal a través de una cánula endotraqueal. A los ratones del grupo de solución salina sólo se les administraron 100 μL de solución salina estéril. Los pasos anteriores se repitieron el 7º día tras la administración. Las CMM sin etiquetar y las CMM etiquetadas (1×106 células por ratón) se colocaron en 100 μL de solución salina y se trasplantaron por vía intratraqueal en los pulmones de los ratones el 10º día tras la primera inyección de BLM. En el grupo PF + MSC marcadas con ASCP-BCN + imán, se fijó un imán de NdFeB al tórax de cada ratón. Los ratones fueron ejecutados el día 28 después de la primera inyección de BLM, y se obtuvieron tejidos pulmonares.
Trasplante de células madre mesenquimales de médula ósea
El día 28, después de la primera inyección de BLM, se pesaron los ratones y se colocaron en un sistema de pletismografía de cuerpo entero WBP para registrar sus datos de función pulmonar. A continuación, se recogieron los pulmones de los ratones para su posterior identificación. Se tomó un lóbulo pulmonar de cada ratón y se limpió suavemente la sangre de su superficie. Se pesó el tejido pulmonar y se horneó a 60°C durante 72 h. Se pesó de nuevo el tejido pulmonar seco y se determinó la relación húmedo-seco del pulmón. La concentración de HYP en el tejido pulmonar se detectó utilizando el kit de detección de HYP.
Efectos terapéuticos
Efectos terapéuticos de las CMM marcadas con ASCP-BCN y la manipulación magnética en la FP
(a) Esquema experimental del tratamiento con CMM del modelo de ratón de FP inducida por bleomicina. (b-e) Función pulmonar de ratones sin tratamiento (control) y modelo de ratones con FP inducida por médula ósea con diferentes tratamientos de (solución salina, MSCs, MSCs marcadas con ASCP-BCN, y MSCs marcadas con ASCP-BCN + manipulación magnética) durante 28 días, luego completar la primera inyección de médula ósea:
(b) Respiraciones por minuto, (c) 50% de capacidad vital de flujo espiratorio, (d) pico de flujo inspiratorio, (e) pico de flujo espiratorio.
(f) Contenido de HYP en el pulmón.
(g) Relación húmedo-seco de los pulmones de cada grupo.
(h) Imágenes representativas de tinción con H&E, imágenes de tinción con tricrómico de Masson e imágenes de tinción inmunohistoquímica con α-SMA de secciones pulmonares de cada grupo.
(i) La gravedad de la PF se evaluó mediante la puntuación de Ashcroft correspondiente a la tinción de H&E.
(j) La tinción con tricrómico de Masson se utilizó para determinar el porcentaje de área de deposición de colágeno pulmonar.
(k) La tinción inmunohistoquímica muestra el porcentaje de células α-SMA positivas.
(l) Análisis por inmunotransferencia de α-SMA y TGF-β en tejidos pulmonares.
(m) Niveles de expresión relativa de las proteínas α-SMA y TGF-β correspondientes.
Efecto terapéutico de las BMSC en la FP
Para evaluar la viabilidad de las BMSC marcadas con ASCP-BCN en el tratamiento de la FP, se utilizó un modelo de FP en ratón inducido por bleomicina (BLM). La intervención con BLM provocó una disminución significativa de la función pulmonar de los ratones, manifestada por un aumento del volumen minuto (VM), el flujo espiratorio al 50% de la capacidad vital (EF50), el flujo inspiratorio máximo (FIP) y el flujo espiratorio máximo (FEP). El trasplante de BMSC redujo ligeramente los parámetros de función pulmonar mencionados. El trasplante de BMSC marcadas con ASCP-BCN y la atracción magnética aliviaron aún más los parámetros de función pulmonar mencionados, lo que indica que desempeña un papel importante en la promoción del efecto terapéutico de las BMSC. En particular, la frecuencia respiratoria y el flujo inspiratorio máximo de los ratones en el grupo de trasplante de CMM marcadas con ASCP-BCN + manipulación magnética casi alcanzaron los del grupo de control. Y lo que es más importante, el trasplante de CMM marcadas y la manipulación magnética no sólo redujeron la concentración de hidroxiprolina (HYP) en los pulmones fibróticos, sino que también redujeron la relación pulmón húmedo/seco causada por la inflamación.
Investigación relacionada
Los resultados se publicaron recientemente en la revista Bioactive Materials (2023, 21, 129) con el título "Cobalt protoporphyrin-induced nano-self-assembly for CT-imaging, magnetic-guidance, and antioxidative protection of stem cells in pulmonary fibrosis treatment".
Enlaces relacionados
https://www.sciencedirect.com/science/article/pii/S2452199X22003383
https://www.sciencedirect.com/science/article/pii/S1748013220300669
Póngase en contacto con nosotros
Nos comprometemos a hacer que su investigación sea más fácil, precisa y eficaz, y a ayudarle a generar confianza en sus datos Hemos prestado servicios a un gran número de clientes, lo que nos ha proporcionado una gran experiencia a la hora de ofrecer soluciones personalizadas y profesionales en función de sus necesidades.