Ver traducción automática
Esta es una traducción automática. Para ver el texto original en inglés haga clic aquí
#Novedades de la industria
El apéndice no sólo puede inflamarse, sino que también puede sufrir cambios cancerosos Puede suponer un riesgo mortal similar al del cáncer colorrectal.
El apéndice no sólo puede inflamarse, sino que también puede sufrir cambios cancerosos Puede suponer un riesgo mortal similar al del cáncer colorrectal.
01
Anatomía y función del apéndice
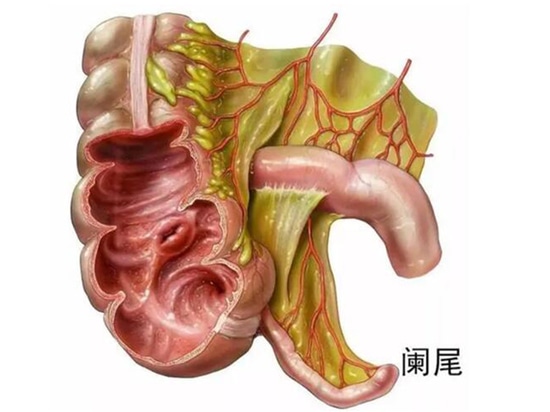
El apéndice es un órgano intraperitoneal, y el peritoneo que lo envuelve forma un mesenterio triangular de doble capa a lo largo de un lado de su pared, conocido como mesenterio apendicular. Por lo tanto, el apéndice es un órgano que se mueve libremente dentro de la cavidad abdominal. Como el mesenterio suele ser más corto que el apéndice, éste tiende a estar enrollado.
El apéndice tiene un aspecto similar al de una lombriz de tierra, con una longitud aproximada de 5 a 10 cm y un diámetro de unos 0,5 cm. Su estructura tisular es similar a la del intestino grueso y consta de cuatro capas de dentro hacia fuera: capa mucosa, capa submucosa, capa muscular y capa serosa. Las capas mucosa y submucosa del apéndice contienen abundante tejido linfoide, lo que convierte al apéndice en un órgano linfoide con ciertas funciones inmunitarias.
Las investigaciones indican que el apéndice participa en la producción y maduración de los linfocitos B. El tejido linfoide del apéndice comienza a aparecer después del nacimiento, alcanza su máximo en la adolescencia, disminuye gradualmente y desaparece por completo después de los 60 años. Por lo tanto, la extirpación del apéndice en adultos no tiene un impacto significativo en la función inmunitaria del organismo.
02
Tumores apendicíticos
La apendicitis es una enfermedad apendicular frecuente, caracterizada por cambios inflamatorios debidos a diversos factores. Es una afección quirúrgica frecuente, más prevalente en individuos jóvenes, con mayor incidencia en varones que en mujeres. La apendicitis aguda es más frecuente clínicamente, afectando a individuos de todas las edades, incluidas las mujeres embarazadas. La apendicitis crónica es menos frecuente.
Tumores/cáncer de apéndice: Aunque la incidencia de tumores apendiculares es baja, existe una tendencia al alza dentro de la población de cánceres del aparato digestivo[1]. Como miembro de la familia de los tumores, a pesar del tamaño aparentemente insignificante de los tumores apendiculares, suponen un riesgo mortal similar al del cáncer colorrectal.
En términos generales, los tumores apendiculares pueden clasificarse en tumores de origen epitelial (como adenomas o adenocarcinomas) y tumores de origen no epitelial (como tumores neuroendocrinos o linfomas). Los tumores apendiculares de origen epitelial se clasifican a su vez en función de la producción de moco, con dos clases distintas que presentan diferencias significativas en el comportamiento biológico y el pronóstico tumoral. La Organización Mundial de la Salud (OMS) denomina neoplasias mucinosas apendiculares de bajo grado (NLAM) a la mayoría de los tumores de origen epitelial no invasivos, que son adenomas bien diferenciados capaces de crecer fuera del apéndice de forma maligna, dando lugar a la acumulación de mucina extracelular. Estas mucinas pueden existir en formas estructurales celulares o no celulares, y estos tumores tienen comportamientos biológicos malignos potenciales, como causar perforación apendicular, fibrosis de la pared apendicular, formación de mucina en la pared apendicular y acumulación de mucina extracelular en los tejidos blandos circundantes. Las neoplasias mucinosas apendiculares de alto grado (HAMN), en comparación con las LAMN, presentan una atipia celular más agresiva.
El tipo más frecuente de tumor de origen no epitelial en el apéndice son los tumores neuroendocrinos (NET). Histológicamente, son similares a los NET de otras partes del aparato digestivo y suelen ser asintomáticos, descubriéndose normalmente de forma incidental tras una apendicectomía. Otros tumores de origen no epitelial poco frecuentes en el apéndice son los tumores del estroma gastrointestinal y los linfomas. La mayoría de los NET de apéndice tienen un estadio tumoral bajo, lo que conlleva un pronóstico relativamente bueno. La tasa de supervivencia a 5 años para pacientes con lesiones localizadas es aproximadamente del 95% al 100%. Aunque el tamaño del tumor está correlacionado con la supervivencia, las investigaciones indican que la tasa de supervivencia global a 5 años no difiere significativamente entre los tumores de menos de 1 cm y los de entre 1 cm y 2 cm. La tasa de supervivencia a 5 años de los tumores mayores de 2 cm se sitúa en torno al 70,5%. Los pacientes con metástasis a distancia tienen una tasa de supervivencia a 5 años inferior al 25%, con una mediana de supervivencia de unos 31 meses.
03
Marcadores de los tumores del apéndice
Adenocarcinoma apendicular: Puede clasificarse en mucinoso y no mucinoso; el adenocarcinoma mucinoso presenta atipia celular de alto grado y más del 50% de las lesiones tienen mucina extracelular[2]. El adenocarcinoma apendicular suele expresar p53, CD44 y CDX2.
Tumores mucinosos del apéndice: Los marcadores tumorales séricos CEA, CA19-9 y CA125 pueden utilizarse para el diagnóstico y la evaluación del estado de la enfermedad de los tumores mucinosos del apéndice. Las mutaciones en los genes KRAS, TP53 y SMAD4 pueden diferenciar entre los HAMN y los LAMN, aunque los expertos creen que no tienen importancia en el diagnóstico o el tratamiento.
04
Tratamiento de los tumores del apéndice
En la actualidad, no existe un consenso unificado sobre el tratamiento de los tumores de apéndice. Los expertos sugieren que el tratamiento de los tumores de apéndice debe basarse en el estado general del paciente, el tipo histopatológico del tumor, la extensión de la afectación y las tendencias evolutivas, siendo la cirugía el principal método de tratamiento[3]
05
Susceptibilidad genética de los tumores de apéndice[4]
Este estudio incluyó a pacientes con cáncer de apéndice que se sometieron a pruebas de mutaciones en la línea germinal de 14 genes de susceptibilidad al cáncer en un laboratorio de pruebas clínicas desde el 1 de marzo de 2012 hasta el 31 de diciembre de 2016. La historia clínica, los antecedentes personales y los antecedentes familiares de los pacientes se obtuvieron de los formularios de solicitud de examen cumplimentados por los médicos clínicos. Se realizaron pruebas multigénicas mediante captura personalizada dirigida, secuenciación y análisis de reordenamiento cromosómico. Los criterios de valoración primarios fueron las mutaciones de línea germinal, la incidencia y el espectro en pacientes con cáncer de apéndice. Las mutaciones de línea germinal en los genes APC, BMPR1A, CDH1, CHEK2, EPCAM, MLH1, MSH2, MSH6, MUTYH, PMS2, PTEN, SMAD4, STK11 y TP53 se asociaron con la susceptibilidad a los cánceres gastrointestinales.
En la cohorte de 131 pacientes con cáncer de apéndice (90 mujeres [68,7%]), 16 pacientes (15,11%) presentaban 5 variantes de secuencia deletéreas. Del mismo modo, cuando se limitó a 74 pacientes con cáncer de apéndice como primer y único tumor primario, 8 pacientes (10,8%) presentaban al menos 1 variante de secuencia deletérea en genes de susceptibilidad al cáncer. En general, se observaron variantes de secuencia deletéreas en 6 pacientes (4,6%) en MUTYH (5 casos con un único alelo MUTYH, 1 caso con un doble alelo MUTYH). Cuatro pacientes con síndrome de Lynch (3,1%) presentaban variantes en la secuencia del gen MLH1, y 3 casos se diagnosticaron a la edad de 50 años o más. Tres pacientes (8,1%) presentaban variantes de secuencia deletéreas en otros genes de susceptibilidad al cáncer (3920 casos en APC [c.1307T>A, p.I2K], 2 casos en CHEK470 [c.157T>C, p.I1T], 4 casos en SMAD263 [c.287 98dup, p.L14IFS*1], 53 casos en TP524 [c.175G>A, p.R<>H]).
Conclusiones: De cada 10 pacientes con cáncer de apéndice sometidos a pruebas de susceptibilidad hereditaria al cáncer, un individuo es portador de mutaciones genéticas asociadas con la susceptibilidad al cáncer. Dada la alta frecuencia y el amplio espectro de variaciones genéticas de la línea germinal, estos datos sugieren que puede ser necesaria una evaluación genética para todos los pacientes diagnosticados de esta rara neoplasia maligna.
Referencias:
[1] Journal of Gastrointestinal Surgery, 2015, 19(4): 743-750.
[2] 4ª ed. Lyon, France: IARC Press, 2010.
[3] Consenso de expertos chinos sobre el tratamiento integral multidisciplinar de los tumores apendiculares (Edición 2021).
[4] JAMA Oncol. 2022 Nov 11;9(1):95-101.
Declaración: Este artículo es sólo para compartir. Si hay algún problema de derechos de autor, póngase en contacto con nosotros lo antes posible y lo corregiremos lo antes posible. Gracias